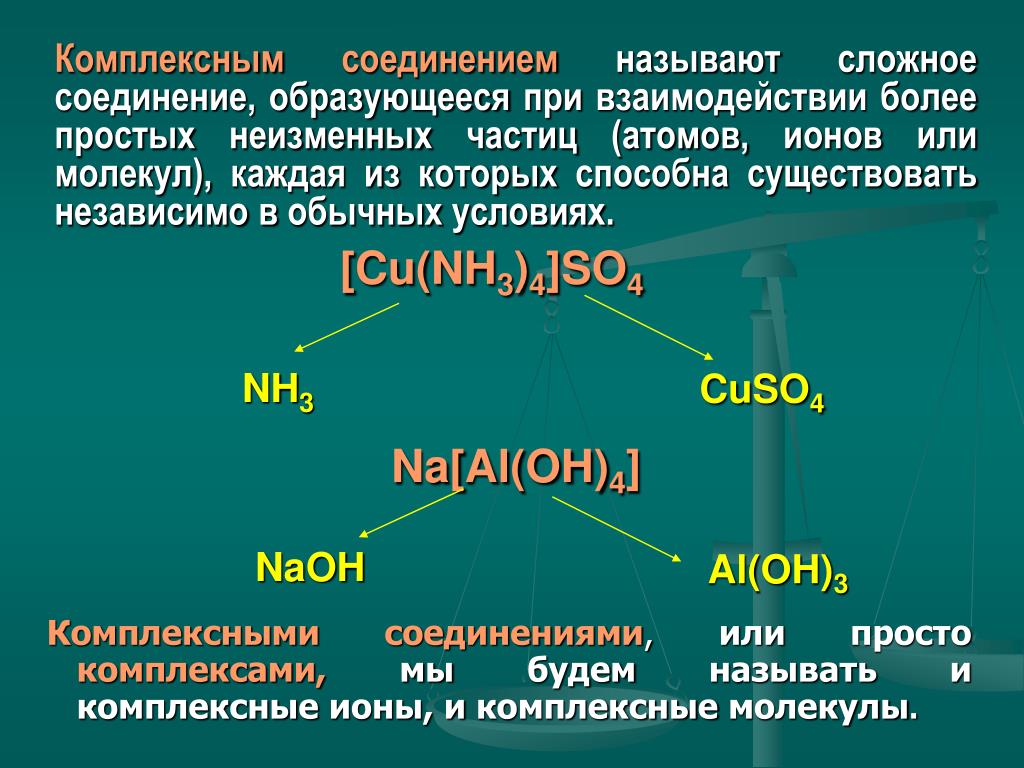
Комплексные соединения – это вещества, состоящие из центрального металлического иона, которому окружающие его атомы и группы атомов связаны координационными связями. Такие соединения обладают широким спектром свойств и находят применение в различных областях науки и техники.
Важной частью изучения комплексных соединений является разработка и определение их систематического названия. Систематические названия позволяют однозначно идентифицировать конкретное соединение и строить закономерности в его свойствах и реакционной способности. Умение правильно называть комплексные соединения является неотъемлемой частью химического образования.
Систематическое название комплексного соединения строится на основе видимой формулы, которая отражает состав и строение. Для каждого элемента в соединении указывается его имя, а через тире – его строение и координационное число. При составлении названия учитывается также заряд комплексного иона, а также указание на имена его лигандов, то есть атомов или групп атомов, которые связаны с центральным металлическим ионом.
Названия комплексных соединений
Комплексные соединения, также известные как координационные соединения, представляют собой соединения, в которых центральный атом или ион образует связи с одним или несколькими другими атомами или ионами, называемыми лигандами. Комплексные соединения могут быть неорганическими или органическими.
Названия комплексных соединений обычно строятся с использованием системы именования, называемой номенклатурой комплексных соединений. Номенклатура комплексных соединений основана на правилах, разработанных Международным союзом по чистой и прикладной химии (IUPAC).
Название комплексного соединения строится следующим образом:
1. Имя лиганда: Первым шагом является определение имени каждого лиганда, связанного с центральным ионом или атомом. Имена лигандов обычно заканчиваются на «-о», если они являются анионами, или на «-а», если они являются нейтральными.
2. Центральный ион или атом: Затем следует указание имени центрального иона или атома. Это имя пишется после имен лигандов.
3. Заряд комплекса: Если комплекс имеет заряд, то он указывается в конце названия, в виде римских цифр или арабских цифр в круглых скобках. Например, (II) или 2+. Если комплекс является нейтральным, заряд не указывается.
Примеры:
Феррицианид калия: цианид калия (CN-) + железо (III) (Fe3+) = цианоферратат калия
Тетраамминкобальт(III) хлорид: аммиак ((NH3)4) + кобальт (III) (Co3+) + хлорид (Cl-) = тетраамминкобальт(III) хлорид
Номенклатура комплексных соединений сложна и требует понимания основных правил. Важно правильно именовать комплексные соединения, чтобы избежать путаницы и облегчить обмен информацией в химической области.
Правила называния соединений
1. Ионные соединения
Для называния ионных соединений необходимо указывать ионы, причем катион указывается первым, а анион – вторым. Катион обозначается названием элемента или группы элементов, а анион – с добавлением суффикса -ид или -ит.
2. Комплексные соединения
Комплексные соединения состоят из центрального иона, так называемого центрального металла, и одной или нескольких лигандов, которые образуют вокруг центрального иона сферу координации. При назывании комплексных соединений указывается имя лиганда и его количество с помощью греческих числительных. Затем указывается имя металла с указанием его степени окисления в римской нотации.
3. Ковалентные соединения
Ковалентное соединение включает в себя атомы, связанные общими электронными парами. При назывании ковалентных соединений указывается название первого элемента и добавляется суффикс -ид. Если в одном соединении присутствуют два одинаковых атома первого элемента, то используется префикс «ди-«, «три-» и так далее. Затем указывается название второго элемента.
Знание правил называния комплексных соединений поможет студентам качественно проводить химические эксперименты, а также лучше понимать химические свойства исследуемых соединений.
Химическая номенклатура комплексных соединений
Номенклатурные правила
Для названия комплексных соединений существуют определенные номенклатурные правила. Они включают в себя указание типа ионов, названия лигандов и порядка их следования, а также указание степени окисления центрального иона.
Номенклатура комплексных соединений обычно строится следующим образом:
- Указание типа ионов: название положительного иона (катиона) ставится перед названием комплексно-образующего иона (аниона), например, «хлорид серебра».
- Названия лигандов: лиганды, образующие координационные связи с центральным ионом, обозначаются специальными названиями, например, «этилендиамин».
- Порядок следования лигандов: если в соединении присутствуют несколько лигандов, их названия указываются в алфавитном порядке.
- Указание степени окисления: степень окисления центрального иона указывается в римской цифре в скобках, например, «(II)».
Примеры
Для наглядности, представим несколько примеров названий комплексных соединений:
- Пентакис(ацетилакетонат)железо(III) — в этом случае пятикратно-координированное комплексное соединение имеет в составе лиганды ацетилакетонат и центральный ион железа с степенью окисления III.
- Тетрахлорид платины(II) — в этом примере комплексное соединение состоит из тетрахлорида платины и центрального иона платины с степенью окисления II.
Химическая номенклатура комплексных соединений позволяет удобно и однозначно называть эти соединения, облегчая коммуникацию в химической науке.
Участие лиганда в названии
Наименование лиганда определяется его названием или псевдонимом, который можно использовать. В зависимости от типа лиганда, определенные правила могут применяться при его наименовании.
Если лиганд является анионом, то его название заключают в квадратные скобки [ ]. Например, [OH] обозначает гидроксидный анион, а [Cl] — хлоридный анион.
Если лиганд является нейтральной молекулой, то его название ставят в скобки (). Например, (NH3) обозначает аммиак, а (H2O) — воду.
Также лиганд может быть ионом, содержащим положительный заряд. В этом случае, его название ставится перед названием комплекса. Например, катион феррия [Fe3+(CN)6]3- образуется от железа и цианида.
Участие лиганда в названии комплексного соединения — важная информация о его структуре и свойствах. Правильное называние лиганда позволяет однозначно определить, с какими веществами он может образовывать комплексы, и какие свойства у этих комплексов могут быть.
| Тип лиганда | Примеры приписывания в названии |
|---|---|
| Анион | [Cl], [OH], [NO3] |
| Нейтральная молекула | (NH3), (H2O), (CO) |
| Ион | [Fe3+(CN)6]3-, [Cu2+(NH3)4]2+ |
Основные типы комплексных соединений
Комплексные соединения представляют собой соединения, в которых центральный металлический ион образует координационную связь с одним или несколькими лигандами. В зависимости от числа и типа лигандов, комплексные соединения могут быть классифицированы следующим образом:
- Моноатомные лиганды:
- — Вода (H2O)
- — Аммиак (NH3)
- — Фосфин (PH3)
- Полиатомные лиганды:
- — Этилендиамин (en)
- — Глицин (gly)
- — Ацетилациклогексанонат (acac)
- Комплексы с несколькими центральными ионами:
- — Димеры
- — Тримеры
- — Тетрамеры
- Изомерические комплексы:
- — Изомерия координационного числа
- — Изомерия геометрии
- Полимерные комплексы:
- — Цепочечный полимер
- — Полимерное кольцо
- — Сетчатый полимер
Знание основных типов комплексных соединений позволяет лучше понять и классифицировать их свойства и реактивность. Кроме того, это имеет важное прикладное значение для разработки новых материалов и катализаторов в различных сферах промышленности и научных исследований.
Названия цветных соединений
В основе названий цветных соединений лежит учет окрашенных ионов, которые добавляются к основному названию соединения. Обычно использование имени иона, который придает цвет соединению, зависит от его заряда. Например, соединение с катионом меди(II), окрашенным в зеленый цвет, будет называться «зеленая медь(II)».
Однако, в некоторых случаях, названия цветных соединений могут быть неочевидными. Например, соединение с анионом феррия, окрашенным в желтый цвет, будет называться «железа(III) фосфат». Такие случаи требуют знания основных правил и изучения номенклатурных таблиц.
Еще одним интересным аспектом названий цветных соединений является использование системы стокситетов. В этой системе соединения указываются с использованием собственных цветовых названий, не зависящих от состава соединения. Например, синий кобальтовый сульфат или зеленая никельовая соль.
В целом, названия цветных соединений могут быть достаточно сложными и требуют хорошего знания номенклатурных правил. Однако, они играют важную роль в разработке и исследовании различных материалов, используемых в различных отраслях науки и промышленности.
Названия координационных соединений

Названия координационных соединений, как правило, строятся на основе имен лиганда и металла. В некоторых случаях, когда лиганд имеет специфические химические свойства, используется название лиганда без изменений, с добавлением слова «комплекс» или «соединение».
Названия на основе ионного радикала лиганда
Некоторые лиганды имеют ионный радикал в своем составе. В таких случаях, название простого лиганда заменяется на название ионного радикала с суффиксом -ато. Например:
| Простой лиганд | Ионный радикал | Название комплексного соединения |
|---|---|---|
| Аммиак | Амм | Аммиачная соль |
| Гидроксид | Гидроксоат | Гидроксокомплекс |
Названия на основе имен химических элементов
Если лигандом является химический элемент, его имя указывается в начале названия координационного соединения с использованием приставки «комплекс» или «соединение». Например:
| Лиганд | Название комплексного соединения |
|---|---|
| Хлорид | Комплекс хлорида |
| Оксид | Соединение оксида |
Это лишь некоторые примеры названий координационных соединений. Конкретное название зависит от типа металла или металлоида, типа и количества лигандов, и других факторов. Важно помнить, что при названии координационных соединений применяются определенные правила, которые позволяют единообразно обозначать их в химических реакциях и научных публикациях.
Ошибка в названии
При названии комплексных соединений, особенно через систематическое номенклатурное правило, может возникнуть ошибка. Ошибка в названии может привести к непониманию или даже к принятию неправильного химического состава комплекса. Установить точное название комплекса крайне важно для понимания его свойств и удобства дальнейшего изучения.
1. Ошибки при определении заряда комплексных соединений
Одна из частых ошибок при названии комплексных соединений – ошибки в определении заряда иона комплекса. Заряд комплекса играет важную роль в его химических свойствах и реакционной способности. Допустить ошибку в определении заряда может привести к некорректному пониманию его химической природы и взаимодействий с другими веществами.
2. Путаница в названии компонентов комплекса
Еще одним источником ошибок при названии комплексных соединений является путаница в названии компонентов комплекса. Необходимо точно знать названия и формулы соединений, которые входят в состав комплекса, чтобы правильно составить его название. Ошибки в названии компонентов могут привести к неверному указанию структуры или химического состава комплекса.
Важно помнить, что ошибка в названии комплексного соединения может привести к неправильному пониманию его свойств и реакционной способности. При названии следует быть внимательным, проверять информацию и не допускать ошибок в определении заряда иона комплекса, а также в названии компонентов комплекса.
Вопрос-ответ:
Какие правила существуют для называния комплексных соединений?
Для называния комплексных соединений существуют определенные правила, основанные на систематическом подходе. Они включают в себя указание типа лиганда, порядкового номера порядка вряд лиганда, ионность комплекса, а также заряд комплекса. Названия также могут включать информацию о структуре комплекса и его свойствах.
Какой тип лиганда необходимо указывать при названии комплексного соединения?
При названии комплексного соединения необходимо указывать тип лиганда. Лиганды могут быть анионами, нейтральными молекулами или катионами, и их названия зависят от химической формулы их самих.
Что такое порядковый номер порядка вряд лиганда?
Порядковый номер порядка вряд лиганда — это число, которое указывает, сколько раз данный лиганд повторяется в комплексе. Он указывается перед названием лиганда. Например, если комплекс содержит два молекулы лиганда, то перед его названием будет указано число 2.
Как указывается ионность комплекса при его названии?
Ионность комплекса указывается при его названии с помощью римских цифр в круглых скобках. Цифра I обозначает неионный комплекс, II — дионный комплекс, III — трионный комплекс и так далее. Ионность комплекса зависит от количества заряженных частей в его составе.
Может ли комплекс иметь заряд?
Да, комплекс может иметь заряд. Заряд комплекса указывается при его названии с помощью арабских цифр и знака «+» или «-«, в зависимости от заряда комплекса. Если комплекс положительно заряженный, то перед его названием будет указан знак «+», а если отрицательно заряженный — то знак «-«.
Что такое комплексное соединение?
Комплексное соединение — это соединение, состоящее из центрального ионного атома, так называемого центра координации, и одного или нескольких лигандов, которые образуют вокруг него координационные связи.
Как называть комплексные соединения?
Названия комплексных соединений строятся по определенным правилам. В названии сначала указывается название лиганда, а затем имя центрального ионного атома. Если количество лигандов больше одного, их названия указываются в алфавитном порядке.