
Спирты — это класс органических соединений, которые являются одними из самых распространенных и важных в химии. Они обладают свойством содержать функциональную группу — группу атомов, которая придает им особенные химические свойства и реакции. Функциональная группа спиртов состоит из гидроксильной (-OH) группы, прикрепленной к углеродному атому в органической молекуле.
Гидроксильная группа является ключевой составляющей спиртов и определяет их классификацию и свойства. Она состоит из атома кислорода, связанного с атомом водорода и углеродным атомом. Гидроксильная группа придает спиртам их характеристическую полярность, растворимость в воде и возможность образования водородных связей.
Функциональная группа спиртов — это одна из самых разнообразных и важных групп в органической химии. Существует множество различных типов спиртов, включая метиловый спирт, этанол, пропанол и многие другие. Они широко используются в промышленности, медицине и быту.
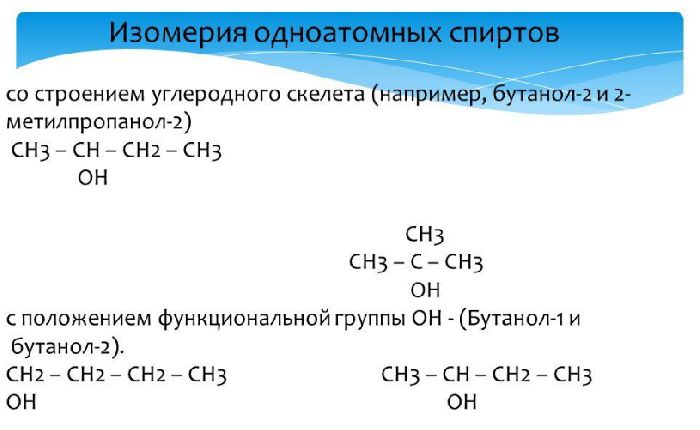
Структура и свойства функциональной группы спиртов
Структура спиртов
Спирты состоят из одного или нескольких углеродных атомов, к которым прикреплена гидроксильная группа. Гидроксильная группа может быть прикреплена к главному цепочке углеродных атомов или к боковой цепи. В зависимости от структуры спиртов можно классифицировать на простые спирты (алкоголи), алифатические спирты и ароматические спирты.
Свойства спиртов
Гидроксильная группа является активным функциональным участком молекулы спирта, что придает ей ряд особых свойств:
- Полярность: Гидроксильная группа содержит электроотрицательный кислородный атом, что делает спирты поларными веществами. Полярность спиртов обуславливает их способность к гидрофильности и способность образовывать водородные связи.
- Растворимость: Малые спирты (с малым числом углеродных атомов) легко растворяются в воде благодаря образованию водородных связей между спиртом и водой. Однако, с увеличением размера спирта, его растворимость в воде снижается.
- Ацидность: Гидроксильная группа в спиртах может выступать как кислотный центр и образовывать водородные связи с базами. Поэтому спирты могут проявлять кислотные свойства.
- Кишечные эффекты: Большинство спиртов обладает свойством разжигать кожу и слизистые оболочки, вызывая ощущение жжения.
Это некоторые из основных свойств и структурных особенностей функциональной группы спиртов, которые делают ее важным и широко используемым классом химических соединений.
Основные типы спиртов и их структурные особенности
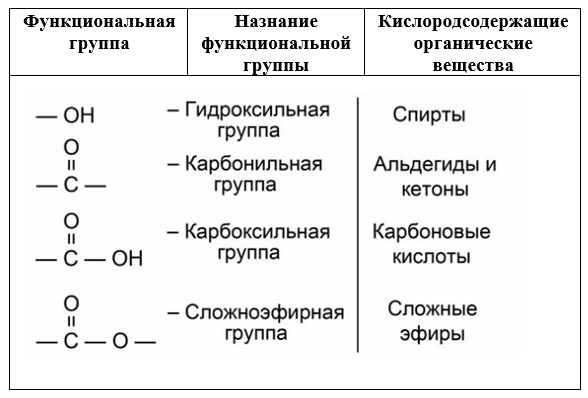
Спирты представляют собой класс органических соединений, в которых группа гидроксила (OH) прикреплена к углеродной цепи. Функциональная группа OH вносит специфические свойства в молекулу спирта, определяющие его химические и физические свойства.
1. Метанол
Метанол (CH3OH) – один из наиболее простых и широко используемых спиртов. У него молекулярная формула СН3ОН, состоящая из одной углеродной атомной цепи и группы гидроксила.
Метанол является токсичным веществом и используется в качестве противозамерзающего агента, растворителя и сырья для производства формальдегида.
2. Этанол
Этанол (С2Н5ОН) – самый известный спирт, который является основным компонентом алкогольных напитков. Он имеет формулу С2Н5ОН и обладает двумя метиловыми группами.
Этанол может быть использован в качестве растворителя, антисептика и топлива.
3. Изопропанол
Изопропанол (C3H7ОН), также известный как изопропиловый спирт, имеет формулу C3H7ОН и состоит из трех углеродных атомов.
Изопропанол широко используется в производстве лакокрасочных материалов, растворителей и антисептиков.
4. Глицерин
Глицерин (C3H5(OH)3) – трехвалентный спирт, имеющий формулу С3Н5(OH)3. У него есть три группы гидроксила.
Глицерин используется в медицине, парфюмерии и производстве косметических продуктов.
Каждый из перечисленных спиртов имеет свои уникальные структурные особенности и применения в различных отраслях промышленности и медицины. Они являются важными соединениями для многих процессов и продуктов, занимающих центральное место в современном обществе.
Физические свойства спиртов и их влияние на химические реакции
Полярность и солватация
Гидроксильная группа делает спирты полярными соединениями. Это означает, что электроны в молекуле спирта не равномерно распределены, и есть разность зарядов. Это свойство спиртов обуславливает их способность к образованию водородных связей с другими молекулами. Спирты могут солватировать другие полярные и ионные соединения, что часто влияет на скорость химических реакций, а также на их механизмы.
Температура кипения и растворимость
Спирты имеют более высокую температуру кипения по сравнению с аналогичными углеводородами. Это объясняется наличием в молекуле спирта гидроксильной группы, которая формирует дополнительные водородные связи и увеличивает межмолекулярные силы. Высокая температура кипения может оказывать влияние на скорость реакций, происходящих в присутствии спиртов.
Также стоит отметить, что спирты обычно растворимы в воде благодаря возможности образования водородных связей между молекулами спирта и молекулами воды. Растворимость спиртов в воде может также влиять на химические реакции, так как спирты могут играть роль растворителей или реагентов в различных системах.
| Физическое свойство | Влияние на химические реакции |
|---|---|
| Полярность | Образование водородных связей и солватация других соединений |
| Температура кипения | Может влиять на скорость реакций и их механизмы |
| Растворимость | Возможность спиртов растворяться в воде и реактивность в различных системах |
Примеры применения спиртов в различных отраслях
Спирты широко используются в различных сферах деятельности человека и играют важную роль в промышленности. Ниже представлены некоторые примеры применения спиртов в различных отраслях:
- Медицина: этиловый спирт является основным компонентом антисептиков и дезинфицирующих средств, которые широко применяются в медицинских учреждениях для обработки ран и инструментов.
- Косметика: спирты часто используются в косметических средствах, например, в лаках для ногтей для быстрого высыхания или в дезодорантах для уничтожения бактерий.
- Пищевая промышленность: этиловый спирт используется в производстве алкогольных напитков, а также как растворитель в процессе изготовления ароматизаторов и экстрактов.
- Энергетика: биотопливо, которое получают из растений, содержит спирты, такие как метанол и этиловый спирт. Они используются в качестве альтернативного источника энергии и могут быть использованы в двигателях внутреннего сгорания.
- Химическая промышленность: спирты являются ценными химическими реагентами и используются в различных химических процессах, например, в производстве пластиков, растворителей и реагентов для синтеза органических соединений.
- Лакокрасочная промышленность: спирты используются в производстве красок и лаков для контроля вязкости, растворения пигментов и достижения требуемых свойств покрытий.
Это лишь некоторые области применения спиртов. В целом, спирты играют неотъемлемую роль в различных отраслях и продолжают находить новые применения.
Токсичность спиртов и меры предосторожности
Одним из основных источников токсичности спиртов является их способность оказывать негативное воздействие на центральную нервную систему. В результате употребления или вдыхания спиртов может возникнуть эффект опьянения, который сопровождается изменением мышления, нарушением координации движений и даже потерей сознания.
Кроме того, спирты могут оказывать токсическое действие на печень, вызывая ее повреждение или даже некроз. Длительное и частое употребление спиртов может привести к развитию хронического алкоголизма, что негативно сказывается на общем состоянии организма и может привести к серьезным заболеваниям.
При работе с спиртами необходимо соблюдать определенные меры предосторожности. Во-первых, следует предусмотреть хорошую вентиляцию помещения, чтобы избежать ингаляции паров спирта. Также рекомендуется использование защитной одежды, рукавиц и средств индивидуальной защиты глаз и дыхания.
В случае попадания спиртов на кожу или в глаза необходимо немедленно промыть их большим количеством воды и обратиться за медицинской помощью. Также рекомендуется избегать приближения спиртов к огню или другим источникам искр, так как они являются зажигательными и могут вызвать пожар.
Итак, токсичность спиртов требует особого внимания и соблюдения мер предосторожности при работе с этими веществами. Необходимо быть внимательным и осторожным, чтобы избежать негативных последствий для здоровья и безопасности.
| Меры предосторожности при работе со спиртами: |
|---|
| Обеспечить хорошую вентиляцию помещения |
| Использовать защитную одежду, рукавицы и средства индивидуальной защиты глаз и дыхания |
| В случае попадания спиртов на кожу или в глаза, обеспечить промывание большим количеством воды и обратиться за медицинской помощью |
| Не допускать приближения спиртов к огню или другим источникам искр |
Спирты как растворители и их совместимость с различными веществами
Особенности спиртов в роли растворителей
Спирты обладают высокой полярностью, что делает их способными растворять поларные и некоторые неполярные вещества. Они могут образовывать взаимодействия с различными функциональными группами, такими как гидроксильные группы, амины и карбонильные группы.
Кроме того, спирты обладают способностью образовывать водородные связи, что позволяет им эффективно растворять вещества, содержащие кислород и азотные группы.
Совместимость спиртов с другими веществами
Спирты обычно хорошо совместимы с водой, что делает их универсальными растворителями в биологических и химических системах. Они также могут растворять некоторые органические и неорганические соединения, такие как кислоты, щелочи, соли и эфиры.
Однако, спирты не всегда совместимы с полимерными материалами, такими как резины и пластмассы. Они могут вызывать опухание, размягчение или разрушение полимерных структур, поэтому перед использованием спиртов имеет смысл провести проверку их совместимости с конкретным материалом.
Спирты как сырье для получения других соединений
Спирты могут быть использованы как реагенты в реакциях замещения, окисления и восстановления. Например, простые спирты могут служить источником нуклеофилов в замещающих реакциях, а можно получить альдегиды или кетоны путем окисления простых или вторичных спиртов.
Кроме того, спирты могут служить сырьем для получения различных соединений, таких как эфиры, эфиры карбоновых кислот, эстеры и ацилгалогениды. Эти соединения могут использоваться в различных областях промышленности и науки в качестве растворителей, ароматизаторов, пластификаторов и прочих веществ.
Таким образом, спирты являются важным сырьем для получения других соединений, и их реакционная способность дает широкий спектр возможностей в органическом синтезе.
Спирты в косметологии и медицине: их свойства и применение
Свойства спиртов
- Высокая растворимость в воде и органических растворителях.
- Противомикробное действие, благодаря способности разрушать клеточные мембраны бактерий и вирусов.
- Антисептическое действие, позволяющее предотвращать развитие инфекций.
- Антиоксидантные свойства, защищающие кожу от свободных радикалов.
- Уникальная способность проникать в глубокие слои кожи, улучшая ее структуру и эластичность.
Применение спиртов в косметологии и медицине
В косметологии спирты широко используются в составе различных средств по уходу за кожей, включая тоники, лосьоны и кремы. Их антисептические свойства помогают бороться с акне и другими проблемами кожи, а антиоксидантные свойства помогают замедлить процесс старения.
В медицине спирты применяются в антисептиках для обработки ран, а также в составе противомикробных препаратов. Они способны уничтожать бактерии и вирусы, предотвращая развитие инфекций.
Однако, несмотря на все положительные свойства спиртов, их использование может вызвать некоторые побочные эффекты, поэтому перед применением следует проконсультироваться с врачом или косметологом.
Вопрос-ответ:
Какую функциональную группу спиртов можно назвать?
Функциональная группа спиртов называется гидроксильная группа.
Что такое функциональная группа спиртов?
Функциональная группа спиртов — это группа атомов или связей в органических молекулах, определяющая их химические свойства. В случае спиртов это гидроксильная группа (-OH).
Каким образом функциональная группа спиртов влияет на свойства органических молекул?
Функциональная группа спиртов, гидроксильная группа, обладает свойствами взаимодействия с другими молекулами, что делает спирты растворимыми в воде и других полярных растворителях. Она также определяет реакционную способность спиртов, так как гидроксильная группа может участвовать в различных химических реакциях, например, образовывать эфиры или участвовать в процессе окисления или превращения в другие функциональные группы.
Какие органические соединения относятся к спиртам?
Органические соединения, содержащие гидроксильную группу (-OH) в своей структуре, относятся к спиртам. Это, например, метанол (CH₃OH), этиловый спирт (C₂H₅OH) и изопропанол (C₃H₇OH).
Почему спирты растворимы в воде?
Спирты растворимы в воде благодаря наличию гидроксильной группы (-OH), которая способна образовывать водородные связи с молекулами воды. Эти водородные связи обеспечивают взаимодействие спиртов с водой и их растворимость.
Как называется функциональная группа спиртов?
Функциональная группа спиртов называется гидроксильная группа или группа гидрокси.
Что такое спирты?
Спирты — это класс органических соединений, которые содержат гидроксильную группу (-OH) как их основную функциональную группу. Спирты могут быть моногидрическими (иметь одну гидроксильную группу) или полигидрическими (иметь две или более гидроксильных групп).