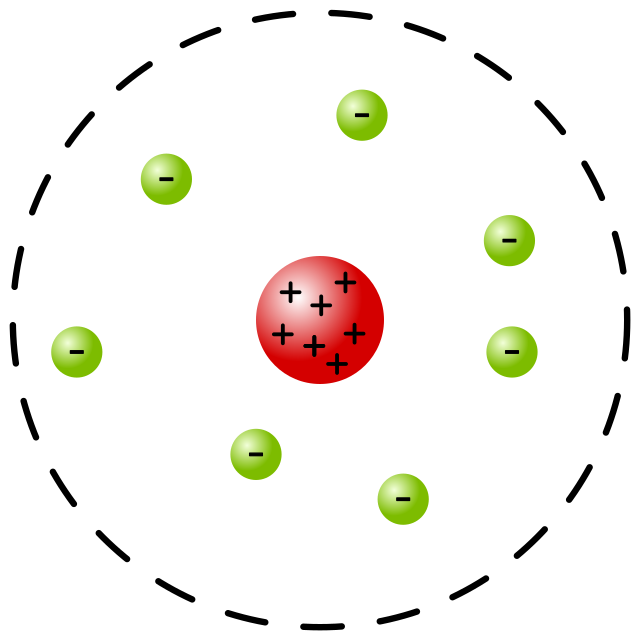
Модель атома Томсона — одна из самых ранних моделей атома, предложенная английским физиком Джозефом Джоном Томсоном в конце XIX века. Она получила название «пудинг с изюмом». Изначально атом рассматривался как неподелимая частица, однако экспериментальные данные свидетельствовали о наличии в нем заряженных частиц.
Основной принцип модели Томсона состоял в том, что атом состоит из положительно заряженного облака, в котором находятся отдельные негативно заряженные частицы, называемые электронами. При этом облако положительно заряжено в целом, так как количество электронов равно количеству положительных зарядов. Эта модель позволяла объяснить некоторые особенности атома, такие как отрицательное влияние электрического поля на лучи катода и их отклонение магнитным полем.
Ключевой момент в модели Томсона заключался в предположении о равномерном распределении электронов внутри положительного облака. Таким образом, атом представлял собой нечто пространственно непрерывное и однородное. Позже эта модель была отвергнута в результате открытия Резерфордом, что атом в основном представляет собой пустое пространство с ядром в центре, окруженным электронами, но она сыграла важную роль в развитии научных представлений о структуре атома.
Модель атома Томсона
Модель атома, предложенная Джозефом Джоном Томсоном в конце XIX века, сыграла важную роль в развитии науки и понимании структуры атома.
По модели Томсона, атом представляет собой неподвижный положительно заряженный шар, внутри которого находятся электроны, распределенные равномерно. Томсон сравнил атом с «рождественским пудингом», где положительный заряд выполнял роль «теста», а отрицательные заряды — «сухофруктов». Это было первым предположением о присутствии электронов внутри атома.
Модель атома Томсона была подтверждена экспериментально через исследование катодных лучей. Томсон обнаружил, что при прохождении электрического тока через трубку с газом, на стенке трубки образуется свечение, а из катода вылетают отрицательно заряженные частицы — электроны. Это подтверждало существование отдельных отрицательно заряженных частиц внутри атома.
Модель Томсона стала первым шагом в понимании структуры атома и проложила путь к дальнейшим исследованиям, в результате которых была разработана модель атома Резерфорда.
| Принципы модели Томсона |
|---|
| 1. Атом состоит из положительно заряженного шара. |
| 2. Внутри атома равномерно распределены отрицательно заряженные электроны. |
| 3. Отрицательный заряд электронов компенсирует положительный заряд атома, делая его электрически нейтральным. |
Название модели Томсона
Модель атома Томсона была предложена ученым Джозефом Джоном Томсоном в конце XIX века и получила название «клубничного пудинга».
По сути, эта модель представляет атом как несжимаемую сферу, внутри которой находятся положительно заряженные частицы, равномерно распределенные по всему объему атома. Эти положительно заряженные частицы называются корпускулями.
Вокруг каждого корпускула находятся отрицательно заряженные электроны, которые равновесно располагаются внутри сферы, чтобы компенсировать положительный заряд корпускул. Электроны похожи на «кленовый сироп», который окружает каждую «клубнику» в пудинге.
Модель Томсона позволяла объяснить радиоактивность и другие экспериментальные данные того времени. Однако она была опровергнута в 1911 году экспериментальными данными Резерфорда, и на смену ей пришла модель Резерфорда-Бора.
Формулировка и название
Одной из первых моделей атома была модель, предложенная Джозефом Джоном Томсоном в 1904 году. Эта модель получила название «пудинг с изюмом». По предложенной Томсоном модели атом представлял собой неподвижный, заряженный позитивным электричеством шар, а отрицательно заряженные электроны находились внутри этого шара, подобно изюминкам в пудинге.
Томсон предложил свою модель для объяснения результатов своих экспериментов, связанных с исследованием разрядов в газовых разрядах. Он обнаружил, что отрицательно заряженные частицы, которые назвал электронами, могут быть отделены от атомов и двигаться в пространстве, что взаимодействие между ними и атомами является основным процессом в газовых разрядах. Согласно модели Томсона, электроны не могут двигаться свободно, а находятся в покое в статическом состоянии внутри атома.
Модель «пудинг с изюмом» Томсона продержалась несколько лет, пока не была заменена моделью Резерфорда, и показала важность понимания атомной структуры и электрической проводимости веществ.
Принципы модели Томсона
1. Атом состоит из электронов, расположенных в положительной среде
Модель атома Томсона предполагает, что атом состоит из небольших и отрицательно заряженных частиц — электронов, которые находятся внутри положительно заряженной среды. Положительная зарядка создается благодаря присутствию протонов в атомном ядре.
2. Атом является электрически нейтральным
В модели Томсона предполагается, что количество электронов в атоме с равно количеству протонов, что делает атом электрически нейтральным в целом. Электроны с отрицательным зарядом и протоны с положительным зарядом компенсируют друг друга, обеспечивая нейтральное состояние атома в целом.
3. Электроны находятся в постоянном движении
Модель Томсона также предполагает, что электроны в атоме находятся в постоянном движении вокруг атомного ядра. Они образуют некий «электронный облако», несущее отрицательный заряд, и находятся в состоянии равновесия с притягивающей их положительной средой.
4. Атом стабилен и не сжимаем
По мнению Томсона, атом является стабильной и несжимаемой единицей. Электроны, двигаясь вокруг атомного ядра, не теряют энергию и не уменьшают свою скорость. Таким образом, атомы могут существовать в стабильном состоянии, без коллапса и сжатия.
В целом, модель Томсона явилась первой попыткой объяснить строение и свойства атома и стала основой для дальнейших исследований и разработок в области атомной физики.
Разделение на заряды
Электромагнитное взаимодействие
Электромагнитное взаимодействие играет ключевую роль в модели атома Томсона, предложенной экспериментальными и теоретическими исследованиями в начале 20 века. Эта модель основывается на представлении атома как непрерывного и несостоятельного электронного облака, которое позитивно заряжено и содержит электроны с отрицательными зарядами.
Электромагнитное взаимодействие между заряженными частицами, такими как электроны и протоны, определяет их взаимное притяжение и отталкивание. В модели атома Томсона электроны находятся в постоянном движении в электронном облаке, подобно планетам, вращающимся вокруг Солнца. Эти движущиеся электроны создают электромагнитные поля, которые взаимодействуют с полями других электронов и протонов.
Электромагнитное взаимодействие влияет на структуру атома Томсона, определяя его размеры и форму. Как и в модели планетарной системы, сила электромагнитного взаимодействия определяется зарядом и расстоянием между заряженными частицами. Заряды разного знака притягиваются друг к другу, а заряды одного знака отталкиваются.
Электромагнитное взаимодействие также играет важную роль в объяснении электронного перехода между энергетическими уровнями атома, что в конечном счете определяет возможность излучения и поглощения электромагнитного излучения атомом.
Важно отметить, что модель атома Томсона с электромагнитным взаимодействием была заменена более современными и точными моделями атома, такими как модель Резерфорда-Бора и модель квантовой механики. Тем не менее, понимание электромагнитного взаимодействия остается важным в области ядерной физики и физики элементарных частиц.
Структура атома
Атом состоит из трех основных частиц: электрона, протона и нейтрона. Электрон обладает отрицательным зарядом и находится вокруг ядра атома. Протон имеет положительный заряд и находится в ядре вместе с нейтроном, который не имеет заряда.
Модель атома Томсона, предложенная в конце XIX века, представляет атом как равновесно заряженную сферу, в которой положительно заряженные протоны равномерно распределены. Отрицательно заряженные электроны находятся внутри этой сферы и создают нейтральность атома в целом. Основными принципами модели Томсона являются равномерное распределение протонов и наличие электронов в атмосфере атома.
Вопрос-ответ:
Как называется модель атома, предложенная Томсоном?
Модель атома, предложенная Томсоном, называется «пудинг с изюмом».
На каких принципах основывается модель атома, предложенная Томсоном?
Модель атома Томсона основывается на следующих принципах: все атомы состоят из положительно заряженного «пудинга», в котором находятся отрицательно заряженные «изюминки».
Почему модель атома Томсона называется «пудинг с изюмом»?
Модель атома Томсона называется «пудинг с изюмом», потому что он представлял себе атомы как сферические структуры с положительным «пудингом» и отрицательными «изюминками», которые в ней находятся.
Каковы основные характеристики модели атома Томсона?
Основные характеристики модели атома Томсона: атомы являются нейтральными, но внутри них сосредоточены отрицательно заряженные частицы, которые называются «электронами».
Какую проблему модель атома Томсона должна была решить?
Модель атома Томсона должна была решить проблему, связанную с тем, каким образом положительный заряд атома согласуется с нейтральностью атома в целом.
Как называется модель атома, предложенная Томсоном?
Модель атома, предложенная Томсоном, называется «пудинг с изюмом».
Какие принципы лежат в основе модели атома, предложенной Томсоном?
Модель атома, предложенная Томсоном, основана на двух принципах: атом состоит из положительно заряженной сферы, внутри которой находятся отрицательно заряженные электроны.