Изотопы — это разновидности атомов одного и того же химического элемента, которые отличаются друг от друга только числом нейтронов в ядре. В то время как атомы одного элемента имеют одинаковое количество протонов, длина существования изотопов может сильно варьироваться. Однако, их физические и химические свойства могут быть очень похожими или вообще неотличимыми.
Изотопы обладают особыми свойствами, которые делают их полезными в различных областях науки и технологии. Например, изотопы используются в радиоактивных исследованиях, в атомной энергетике и в медицине. Изотопы также помогают ученым исследовать происхождение и эволюцию Земли и жизни на ней.
Что такое изотопы и как они образуются
:no_upscale()/imgs/2019/08/13/13/3514910/462e96e4558d7c474c3ac4a0cc4b7ee70bd6f96c.jpg)
Как образуются изотопы
Изотопы образуются в результате взаимодействия нейтронов и протонов в ядре атома. При этом может происходить изменение количества нейтронов в ядре, что приводит к образованию нового изотопа.
Существует несколько способов образования изотопов:
1. Радиоактивный распад — при этом процессе ядро нестабильного изотопа распадается на более стабильные элементы с меньшим количеством нейтронов. В результате образуется новый изотоп.
2. Ядерные реакции — при этом процессе ядро испытывает различные реакции, в результате которых может произойти изменение количества нейтронов. Например, ядро может захватить нейтрон и превратиться в новый изотоп.
3. Синтез атомов — в лабораторных условиях можно создать новые изотопы путем взаимодействия атомов разных элементов.
Изотопы имеют различные свойства и применяются в разных областях науки и техники. Некоторые изотопы являются радиоактивными и используются в медицине для диагностики и лечения различных заболеваний. Другие изотопы используются для исследования природных процессов, а также в промышленности и сельском хозяйстве.
| Изотоп | Массовое число |
|---|---|
| Углерод-12 | 12 |
| Углерод-13 | 13 |
| Углерод-14 | 14 |
В таблице приведены примеры изотопов углерода и их массовые числа.
Определение и примеры изотопов
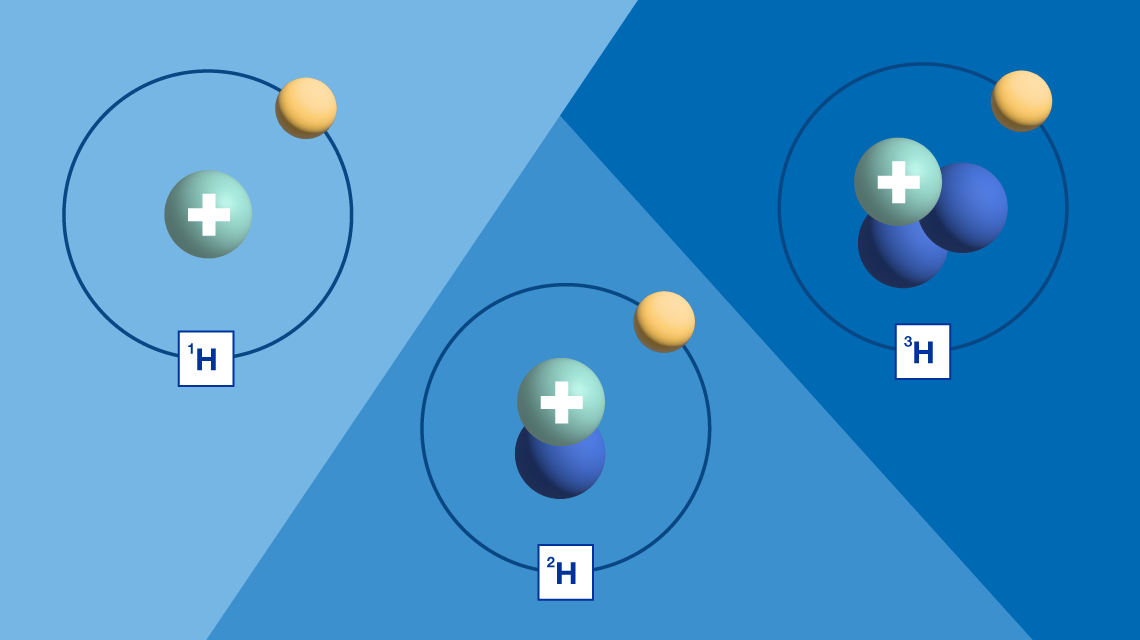
Примером изотопа является водород. У обычного атома водорода в ядре есть один протон и нет нейтронов, обозначается он символом 1H. В то время как у дейтерия, являющегося изотопом водорода, в ядре присутствует один протон и один нейтрон, обозначается он символом 2H.
Еще одним примером изотопа является углерод. В нормальных условиях углерода в ядре содержатся 6 протонов и 6 нейтронов, обозначается он символом 12C. В то время как углерод-14, являющийся изотопом углерода, содержит в ядре также 6 протонов, но уже 8 нейтронов, обозначается он символом 14C.
Таким образом, изотопы могут отличаться по массовому числу, образуя разные разновидности атомов одного элемента. Изотопы имеют одинаковые химические свойства, однако могут иметь различные физические свойства.
Процесс образования изотопов
Изотопы образуются в результате ядерных реакций и процессов внутри атомного ядра. В основном, изотопы образуются путем изменения числа нейтронов в атоме.
Ядерные реакции
Ядерные реакции могут привести к образованию новых изотопов. Они могут быть искусственными, когда атомы бомбардируются частицами, или естественными, когда происходят внутри звезд или в результате радиоактивного распада.
В искусственных ядерных реакциях, частицы нейтронов или протонов могут быть захвачены или выброшены из атома, в результате чего меняется его массовое число и образуется новый изотоп.
Радиоактивный распад
При радиоактивном распаде, ядро нестабильного атома испускает частицу или энергию, чтобы достичь более стабильного состояния. Это может привести к образованию нового изотопа, когда число протонов или нейтронов изменяется.
Изотопы, образованные путем радиоактивного распада, могут быть радиоактивными сами по себе или переходить в другие изотопы путем дополнительного распада.
В обоих случаях, процесс образования изотопов является непредсказуемым и может происходить при определенных условиях. Каждый изотоп имеет свои уникальные свойства и может играть важную роль в различных научных и технических областях.
Основные характеристики изотопов
1. Массовое число
Одной из основных характеристик изотопов является их массовое число, которое равно сумме протонов и нейтронов в ядре атома. Массовые числа различных изотопов одного элемента могут различаться, что приводит к разной атомной массе.
2. Атомная масса
Атомная масса – это среднее значение массового числа для всех изотопов данного элемента, учитывая их естественное распределение в природе. Атомная масса указывается в периодической системе элементов и измеряется в атомных единицах массы (аму).
Изотопы обладают различными свойствами и могут иметь разный эффект на химические и физические процессы. Например, некоторые изотопы являются радиоактивными и обладают нестабильностью, что позволяет их использовать в медицине и науке.
Особенности радиоактивных изотопов
Одна из особенностей радиоактивных изотопов – их нестабильность. Из-за превышения числа нейтронов над протонами в ядре, они стремятся достичь стабильности путем испускания радиоактивных частиц. Это происходит в процессе радиоактивного распада, который может быть альфа-, бета- или гамма-распадом.
Радиоактивные изотопы имеют различные полезные применения в науке, медицине и промышленности. Они используются в радиоизотопной диагностике, радиотерапии и в процессе проведения исследований в радиохимии и радиоэкологии. Благодаря их уникальным свойствам, радиоактивные изотопы являются важными инструментами для изучения и понимания различных процессов и явлений.
Что такое радиоактивность и как она проявляется в изотопах
Когда изотоп неравновесен, ядро стремится достичь более стабильного состояния. Для этого оно подвергается радиоактивному распаду, при котором выделяется энергия и выбрасываются частицы. Процесс распада может быть спонтанным, или стимулированным внешними факторами, такими как радиационная нагрузка или теплота.
Тип радиационного излучения, которое испускает радиоактивный изотоп, может варьироваться. Он может включать альфа-частицы, бета-частицы, гамма-лучи, нейтроны и другие формы излучения. Каждая форма радиационного излучения имеет различную проникающую способность и эффект на окружающую среду и живые организмы.
Радиоактивность может иметь как положительные, так и отрицательные последствия. С одной стороны, радиоактивные изотопы выступают важным инструментом в науке и медицине, используемыми, например, для диагностики и лечения заболеваний. С другой стороны, большое количество радиоактивных изотопов может представлять опасность для здоровья и окружающей среды, излучая вредную радиацию и приводя к мутациям в ДНК.
Изучение радиоактивности и ее проявления в изотопах важно для понимания ядерной физики, а также для разработки мер безопасности и эффективных методов использования радиоактивных материалов в науке и промышленности.
Использование радиоактивных изотопов в науке и медицине
Использование радиоактивных изотопов в науке
В науке радиоактивные изотопы применяются для проведения различных исследований. Они могут использоваться для определения возраста геологических объектов, изучения скорости химических реакций, исследования состава веществ и др. Также радиоактивные изотопы используются в атомной энергетике для производства электроэнергии и создания ядерного оружия.
Использование радиоактивных изотопов в медицине
В медицине радиоактивные изотопы нашли широкое применение. Они используются, например, для проведения радиоизотопного сканирования, которое позволяет клиническим врачам получать диагностическую информацию о состоянии органов и тканей пациента. Также радиоактивные изотопы высоких энергий применяются в радиационной терапии для лечения различных видов рака.
Для обозначения радиоактивных изотопов в науке и медицине используют знаки, показывающие химический элемент и его массовое число. Например, радиоактивный изотоп урана, имеющий 235 нейтронов в ядре, обозначается как U-235.
| Изотоп | Применение |
|---|---|
| Углерод-14 | Используется для определения возраста археологических находок и датирования ископаемых останков. |
| Йод-131 | Применяется в радиоизотопной терапии для лечения рака щитовидной железы. |
| Кобальт-60 | Используется в радиационной терапии для лечения различных видов рака. |
Использование радиоактивных изотопов в науке и медицине продолжает развиваться, открывая новые возможности для диагностики и лечения различных заболеваний. Вместе с тем, необходимы строгие меры контроля и безопасности при работе с радиоактивными веществами, чтобы минимизировать риски для здоровья человека и окружающей среды.
Значение изотопов для понимания истории Земли
Изотопы играют важную роль в науке и позволяют ученым раскрыть тайны истории Земли. Благодаря изотопам, мы можем понять, какая была атмосфера нашей планеты миллионы лет назад, какие были климатические условия и какие процессы происходили на поверхности Земли.
Изотопы и геологические процессы
Изотопы помогают ученым изучать различные геологические процессы, такие как геологические перемещения, вулканизм, эрозия и накопление отложений. Например, изотопы углерода могут указывать на изменения климата и возникновение ледниковых периодов.
Также, изотопы помогают ученым определить возраст горных пород и археологических находок с помощью радиоактивного датирования. Это позволяет узнать, когда и какие события происходили в прошлом Земли.
Изотопы и биологические процессы
Изотопы играют важную роль в изучении биологических процессов. Например, изотопы кислорода и водорода могут помочь в понимании водного круговорота и соединения воды, что позволяет ученым изучать экосистемы и водные ресурсы.
Также, изотопы углерода используются в изучении процессов фотосинтеза и питания растений. Это позволяет ученым понять, какие растения существовали в прошлом и как происходило их развитие.
Использование изотопов для определения возраста геологических образований
Каждый изотоп имеет свой собственный период полураспада, то есть время, через которое половина атомов данного изотопа превратится в атомы другого элемента. Используя эту особенность, геологи могут определить возраст геологических образований с помощью радиоизотопных методов.
Одним из таких методов является радиоуглеродное датирование. Радиоуглеродный метод основан на изотопе углерода-14, который постепенно образуется в верхних слоях атмосферы Земли. Когда растение или животное умирает, набор атомов углерода в его организме прекращается, и со временем углерод-14 начинает распадаться на углерод-12. Измеряя количество углерода-14 и углерода-12 в останках, геологи могут определить время, прошедшее с момента смерти организма.
Другим распространенным методом является датирование по изотопу плутония-238 и его продуктов распада. Плутоний-238 изначально образуется в магме горных пород, и с течением времени распадается на другие элементы, такие как уран, торий и радий. Измеряя содержание плутония-238 и его продуктов распада в геологических образцах, геологи могут определить их возраст.
Таким образом, использование изотопов позволяет геологам определить возраст геологических образований с большой точностью. Это помогает понять историю Земли, изучить геологические процессы и предсказывать будущие изменения в окружающей среде.
Роль изотопов в изучении климатических изменений
Изотопы играют важную роль в изучении климатических изменений. Изотопные анализы позволяют ученым получить информацию о прошлых климатических условиях и предсказать будущие изменения.
Что такое изотопы и как они связаны с климатом
Изотопы — это атомы одного и того же элемента, но с разным числом нейтронов. Некоторые изотопы являются радиоактивными и могут использоваться для определения возраста геологических образцов или истории климатических изменений. Климат оказывает влияние на состав атмосферы, водных ресурсов и океанов, что в свою очередь отражается в изотопной составляющей этих систем.
Палеоклиматология и изотопные анализы
Изотопные анализы могут помочь палеоклиматологам в изучении прошлых климатических изменений. Они анализируют изотопы в геологических образцах, таких как ледниковые керны, каротажные отложения или коралловый скелет, чтобы понять, какие климатические условия были в прошлом.
Например, изотопный анализ керна льда позволяет ученым получить информацию о температуре и атмосферных условиях в прошлом. Путем изотопного анализа карбонатов морских раковин можно определить, какие были уровни моря в прошлые времена.
Прогнозирование климатических изменений с помощью изотопов
Изотопы также используются для прогнозирования будущих климатических изменений. Анализ изотопного состава углерода в атмосфере позволяет ученым определить источники выбросов углерода и установить связь между уровнем парниковых газов и изменением климата.
Также изотопы водорода и кислорода в молекулах воды используются для изучения цикла воды и изменений водных ресурсов в связи с климатом.
Таким образом, изотопы играют важную роль в понимании климатических изменений прошлого и способствуют прогнозированию будущих изменений. Изотопные анализы помогают нам лучше понять и оценить последствия климатических изменений для нашей планеты.
Вопрос-ответ:
Что такое изотопы?
Изотопы — это атомы одного и того же элемента, которые имеют одинаковое число протонов, но разное число нейтронов в ядре.
Какие изотопы существуют?
Существует огромное количество изотопов, для каждого химического элемента существует несколько изотопов.
Как изотопы используются в науке?
Изотопы используются, например, для радиоуглеродного метода определения возраста артефактов или для проведения медицинских исследований.
Могут ли изотопы иметь разные химические свойства?
Изотопы имеют равные химические свойства, так как их электронные структуры одинаковы.
Можно ли создать новые изотопы искусственным путем?
Да, современная наука изучает создание новых изотопов методом ядерно-физических реакций.
Что такое изотопы?
Изотопы — это атомы одного и того же химического элемента, у которых отличается число нейтронов в ядре. Таким образом, изотопы имеют одинаковое количество протонов, но разное количество нейтронов.
Какие изотопы бывают?
Существует несколько типов изотопов: стабильные изотопы, радиоактивные изотопы и изотопы с очень долгим периодом полураспада. Стабильные изотопы не подвержены распаду и их ядра стабильны. Радиоактивные изотопы имеют нестабильные ядра, которые распадаются со временем, излучая радиацию. Изотопы с очень долгим периодом полураспада имеют ядра, которые распадаются очень медленно, и поэтому считаются практически стабильными.