
Атомы, как известно, являются основными строительными блоками материи. В обычных условиях атомы находятся в состоянии, называемом нормальным. В данном состоянии электроны, находящиеся на орбиталях вокруг ядра, находятся в своих нижайших энергетических уровнях.
Однако, при получении энергии внешним воздействием, атомы могут перейти в возбужденное состояние. Возбуждение атома происходит, когда электроны поглощают энергию и поднимаются на более высокие энергетические уровни. Возбужденный атом временно находится в неустойчивом состоянии и ищет способ избавиться от избыточной энергии.
Избавление от избыточной энергии происходит через испускание фотона, маленького пакета энергии в виде электромагнитных волн. Таким образом, атом возвращается в свое нормальное состояние. Процесс испускания фотона называется спонтанным излучением.
Важно отметить, что возбужденное состояние атома может быть достигнуто не только внешним воздействием, но и в результате внутренних переходов электронов между энергетическими уровнями. Это наблюдается, например, при освещении атома электромагнитным излучением определенной частоты.
Состояния атома: нормальное и возбужденное
Нормальное состояние
В нормальном состоянии атом находится в основном энергетическом уровне. В этом состоянии электроны находятся в стабильном электронном облаке с определенными атомными орбиталями. Каждый энергетический уровень имеет определенное количество электронов, которые заполняют его по определенным правилам. В нормальном состоянии атом не поглощает и не излучает энергию.
Возбужденное состояние
Атом может перейти в возбужденное состояние, когда поглощает энергию, например, от столкновения с другим атомом или от поглощения фотона света. В возбужденном состоянии электроны переходят на более высокие энергетические уровни или даже покидают атом. При возвращении в нормальное состояние атом излучает избыточную энергию в виде фотона света или тепла.
Переходы атома между нормальным и возбужденным состоянием играют важную роль в различных физических и химических процессах, включая спектральный анализ и химические реакции.
Что такое атом?
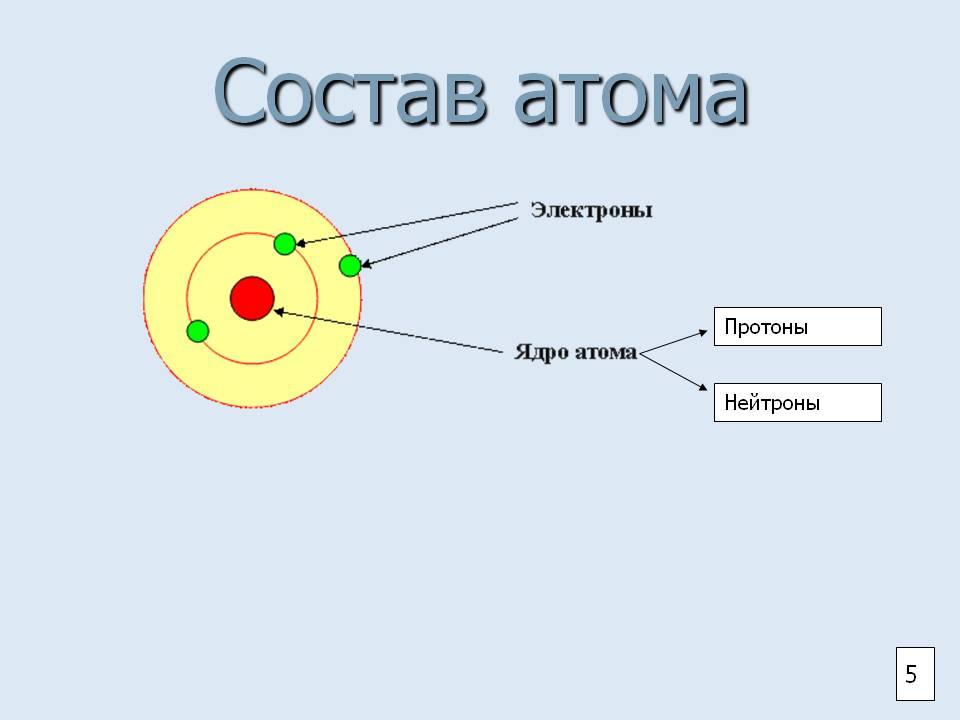
Протоны — элементарные частицы с положительным зарядом, находящиеся в ядре атома. Нейтроны — также элементарные частицы, но не имеющие заряда. Электроны — отрицательно заряженные частицы, которые обращаются вокруг ядра на определенных энергетических уровнях.
Атом в нормальном состоянии имеет свои энергетические уровни и орбитали, которые соответствуют определенным значениям энергии электрона. Когда атом поглощает энергию, электроны могут переходить на более высокие энергетические уровни, что приводит к возбуждению атома.
Возбужденное состояние атома не является устойчивым и электроны стремятся вернуться на более низкие энергетические уровни. При этом они испускают энергию в виде фотонов, что приводит к излучению света или других форм излучения, в зависимости от частоты энергии.
Возбуждение атома может происходить при взаимодействии с другими атомами, молекулами или электромагнитным излучением. Таким образом, нормальное состояние атома соответствует его основному энергетическому уровню, а возбужденное состояние — энергетическому уровню, выше основного.
Структура атома
Атом представляет собой основную единицу любого химического элемента. Он состоит из трех основных частей: ядра, электронной оболочки и электронов.
Ядро атома
Ядро атома содержит протоны и нейтроны. Протоны имеют положительный электрический заряд, а нейтроны не имеют заряда. Поэтому ядро атома обладает положительным общим зарядом. Протоны и нейтроны называются нуклонами.
Число протонов в ядре, называемое атомным номером, определяет химические свойства элемента и определяет его положение в таблице Менделеева.
Массовое число атома — это сумма протонов и нейтронов в ядре.
Электронная оболочка
Электронная оболочка окружает ядро атома и состоит из электронов. Электроны имеют отрицательный электрический заряд и вращаются по орбитам вокруг ядра.
Электроны находятся на разных энергетических уровнях, ближайший к ядру энергетический уровень называется первым, затем идут второй, третий и так далее.
Нормальное состояние атома
Атом находится в нормальном состоянии, когда все его электроны находятся на минимально возможных энергетических уровнях.
Возбужденное состояние атома
Атом переходит в возбужденное состояние, когда один или несколько его электронов переходят на более высокие энергетические уровни. Это происходит, когда атом поглощает энергию от внешнего источника, такого как тепло или свет. Возбужденное состояние атома нестабильно и атом стремится вернуться в нормальное состояние, испустив избыточную энергию в виде фотонов света.
Что такое нормальное состояние атома?
В нормальном состоянии атома, электроны располагаются вокруг ядра на определенных орбиталях, которые соответствуют разным энергетическим уровням. Наиболее близкие к ядру орбитали имеют наименьшую энергию и называются 1s, затем следуют 2s, 2p, 3s и так далее.
Когда атом находится в нормальном состоянии, электроны занимают наиболее низкое энергетическое состояние, обладают минимальной возможной энергией и не переходят на более высокие энергетические уровни без воздействия внешней энергии.
При нагревании или другом воздействии атом может перейти в возбужденное состояние, при котором электроны получают энергию и перемещаются на более высокие энергетические уровни. Возбуждение атома может происходить под воздействием тепла, света, электрического разряда и других факторов.
Возбужденное состояние атома не является устойчивым и длится недолго. Электроны в возбужденном атоме скоро возвращаются в свои основные энергетические уровни, испуская энергию в виде света или других форм электромагнитного излучения в процессе спонтанного излучения или стимулированного испускания.
Нормальное состояние атома является его устойчивым и состоит из электронов, занимающих основные энергетические уровни. Оно является отправной точкой для изучения взаимодействия атомов с внешней средой и предоставляет основу для многих химических и физических процессов.
Как происходит возбуждение атома?
Возбуждение атома происходит при передаче энергии атому из внешнего источника, например, при воздействии света, электромагнитного поля или при столкновении с другими атомами или молекулами.
Атом обладает нормальным состоянием, когда его электроны находятся в наименьшей энергетической области, или энергетическом уровне. В нормальном состоянии электрон обычно находится в основном энергетическом состоянии, ближайшем к ядру атома.
Однако, при воздействии энергии, электроны могут перемещаться на более высокие энергетические уровни, что и называется возбуждением атома.
Возбуждение атома может происходить на различные способы. Например, при поглощении фотона света электрон атома, находящийся на нижнем энергетическом уровне, может переместиться на один из более высоких энергетических уровней.
Кроме того, возбуждение атома может происходить при столкновении с другими атомами или молекулами, при котором энергия передается от одного атома к другому.
После того, как атом был возбужден, электрон может оставаться на более высоком энергетическом уровне некоторое время, прежде чем вернуться к нормальному состоянию. При этом, электрон испускает избыточную энергию в виде света или других форм электромагнитного излучения. Это явление называется флюоресценцией или люминесценцией.
Таким образом, возбуждение атома играет важную роль во многих процессах, включая фотохимические реакции, спектроскопию и генерацию света в различных источниках освещения.
Энергетические уровни атома
Атом состоит из полностью заполненных энергетических уровней, на которых находятся электроны. Каждый уровень имеет определенную энергию, связанную с движением электрона вокруг ядра.
Нормальным состоянием атома считается такое, при котором электроны находятся на своих основных энергетических уровнях, ближайших к ядру. В нормальном состоянии атом стабилен и не обладает энергией, способной к передаче или излучению.
Однако атом может быть возбужден, то есть перейти в состояние, при котором электроны перемещаются на более высокие энергетические уровни. Это может произойти при поглощении энергии в виде света, тепла или других внешних воздействий. Возбужденный атом обладает избыточной энергией, которую он может передавать другим атомам или излучать в виде света.
Переход электронов между энергетическими уровнями происходит с определенной энергией, которая соответствует разнице между уровнями. Эта энергия связана с определенным спектральным фотоном света, что позволяет установить энергетическую структуру атома и проводить спектральный анализ вещества.
Таким образом, энергетические уровни атома определяют его состояние и свойства, позволяя анализировать источники излучения света, а также взаимодействие веществ с внешними факторами.
Излучение при переходе атома из нормального состояния в возбужденное
Переход атома из нормального состояния в возбужденное сопровождается излучением энергии в виде фотонов. Когда атом получает достаточно энергии, его электроны могут перейти на более высокие энергетические уровни. Это происходит благодаря поглощению энергии от внешнего источника, например, при возбуждении электронов путем нагрева.
Возбужденные электроны находятся в неустойчивом состоянии и стремятся вернуться к своей нормальной энергетической уровень. В процессе возвращения электроны излучают энергию в виде фотонов. Частота излученного фотона определяется разностью энергетических уровней между нормальным и возбужденным состояниями атома.
| Состояние атома | Описание |
|---|---|
| Нормальное состояние | Состояние, в котором электроны находятся на своих низших энергетических уровнях. |
| Возбужденное состояние | Состояние, в котором электроны получили достаточно энергии и перешли на более высокие энергетические уровни. |
Излучение при переходе атома из нормального состояния в возбужденное имеет большое значение в физике и химии. Это позволяет исследовать электронные переходы, спектральные линии и оптические свойства вещества. Изучение излучения при переходе атома из нормального состояния в возбужденное также находит применение в различных технологиях, включая лазеры, флуоресцентные лампы и фотоэлементы.
Особенности возбужденных состояний атомов
Атомы могут находиться в двух состояниях: нормальном (основном) и возбужденном. Нормальное состояние атома характеризуется тем, что все его электроны занимают свои основные энергетические уровни, близкие к ядру. В этом состоянии атом наиболее стабилен и не проявляет способности к химическим и физическим реакциям.
Возбужденное состояние атома возникает, когда электрон получает энергию и переходит на высший энергетический уровень. Возбуждение может происходить различными способами, например, при взаимодействии с фотонами или при столкновениях с другими частицами. При переходе электрона на более высокий уровень атом становится нестабильным и готов к химическим и физическим реакциям.
Особенности возбужденных состояний атомов связаны с изменением их энергетической структуры. Возбужденный атом имеет большую энергию, чем атом в нормальном состоянии. При этом возбужденные электроны могут находиться на любом из доступных им энергетических уровней, включая уровни, на которых они не могут находиться в нормальном состоянии.
Состояние возбужденного атома является переходным и недолговечным. Электрон, находящийся в возбужденном состоянии, имеет склонность к возвращению на основной энергетический уровень. При этом энергия, полученная электроном в возбужденном состоянии, может быть излучена в виде фотона. Это явление называется спонтанным излучением.
Возбуждение атомов играет важную роль во многих физических и химических процессах. Оно может вызывать испускание света, как в случае с фосфоресценцией или люминесценцией, а также является ключевым моментом в работе лазеров и фотоэлектрических элементов.
| Особенности возбужденных состояний атомов |
|---|
| 1. Атомы в возбужденных состояниях имеют большую энергию по сравнению с атомами в нормальном состоянии. |
| 2. Возбужденные электроны могут находиться на различных энергетических уровнях, включая уровни, на которых они не могут находиться в нормальном состоянии. |
| 3. Возбужденное состояние атома является переходным и нестабильным. |
| 4. Возбуждение атомов важно для работы лазеров, фотоэлементов и других устройств. |
Важность изучения и применения возбужденных состояний атомов
Атомы, как основные строительные блоки вещества, могут находиться в двух основных состояниях: нормальном и возбужденном. Возбужденное состояние атома характеризуется тем, что энергетический уровень его электрона принимает значение выше обычного, или «основного» уровня. Это возможно благодаря приобретению атомом дополнительной энергии, например, при воздействии на него электромагнитного излучения.
Изучение возбужденных состояний атомов является важной областью науки и находит применение в различных сферах. Одной из таких сфер является астрофизика. С помощью спектроскопии, метода анализа излучения от атомов в возбужденных состояниях, ученые могут изучать состав и свойства межзвездного вещества, а также процессы, происходящие в космосе. Помимо этого, изучение атомов в возбужденных состояниях помогает ученым определить состав и свойства планет, звезд и галактик.
Возбужденные состояния атомов также находят применение в технологии. Например, в лазерных системах используется свойство атомов переходить из возбужденного состояния в основное и при этом излучать фотоны с определенной длиной волны. Это позволяет создавать лазеры различной спецификации, которые находят применение в медицине, научных исследованиях, коммуникации и других областях.
Возможности контроля и манипулирования атомами в возбужденных состояниях
Изучение и применение возбужденных состояний атомов также позволяет ученым контролировать и манипулировать свойствами атомов. Например, путем управления процессом возбуждения и релаксации атомов можно увеличивать или уменьшать их способность к поглощению или испусканию света. Это имеет значение, например, в фотонике и оптоэлектронике, где работа с атомами в возбужденных состояниях позволяет создавать устройства для усиления, фильтрации и модуляции света.
Последствия возбужденных состояний атомов
Также стоит отметить, что возбужденные состояния атомов могут иметь важные последствия для биологических систем. Например, уровень возбуждения атомов и молекул в организме может влиять на реакции и процессы в клетках и тканях. Изучение этих состояний может помочь в понимании биологических механизмов и разработке новых методов диагностики и лечения различных заболеваний.
Таким образом, изучение и применение возбужденных состояний атомов имеет большую важность в различных областях науки и технологии. Это позволяет ученым расширить наши знания о природе и устройстве вещества, а также разработать новые технологии и методы, которые могут быть полезными во многих сферах жизни.
Вопрос-ответ:
Что такое нормальное состояние атома?
Нормальное состояние атома — это состояние, в котором его электроны находятся на наименьшей энергетической орбитали и не испытывают внешнего воздействия, то есть не возбуждены.
Что такое возбужденное состояние атома?
Возбужденное состояние атома — это состояние, в котором его электроны переходят на более высокие энергетические орбитали под воздействием внешних факторов, таких как теплота, свет или электрическое поле.
Какие факторы могут привести к возбуждению атома?
Факторы, которые могут привести к возбуждению атома, включают в себя поглощение света определенной длины волны, облучение атома высокоэнергетическими частицами или атомами, а также повышение температуры или воздействие электрического поля.
Как можно определить, находится ли атом в нормальном или возбужденном состоянии?
Состояние атома можно определить по спектру испускаемого или поглощаемого им света. Если атом находится в нормальном состоянии, то он будет испускать или поглощать свет только определенных длин волн. Возбужденный атом, наоборот, будет испускать или поглощать свет на различных длинах волн.
Какое значение имеет возбужденное состояние атома?
Возбужденное состояние атома имеет большое значение в физике и химии, так как при переходе атома из возбужденного состояния в нормальное происходит испускание или поглощение света определенных длин волн, что позволяет изучать состав и свойства веществ.
Что значит, когда атом находится в нормальном состоянии?
Атом считается находящимся в нормальном состоянии, когда его энергетические уровни соответствуют основному состоянию. В основном состоянии энергия электронов на самом нижнем энергетическом уровне и они не возбуждены.