Закономерности, связанные с изменением физических свойств веществ при изменении внешних условий, всегда представляли интерес как для ученых, так и для обычных людей. Например, все мы знаем, что вода при нагревании до определенной температуры начинает закипать.
Температура, при которой происходит закипание жидкости, называется точкой кипения. Данное явление является одним из основных свойств жидкостей и позволяет использовать их в различных сферах деятельности человека, например, при приготовлении пищи или производстве пара.
Точка кипения жидкости зависит от множества факторов, таких как давление, состав вещества и чистота жидкости. Однако для большинства веществ существуют определенные условия, при которых они будут закипать. Именно эта температура называется температурой кипения и является значимым показателем в химии и физике.
Атмосферное кипение
Температура, при которой начинается атмосферное кипение, зависит от давления вокруг жидкости и данное давление определяется географическим расположением места. На уровне моря, при нормальных условиях, вода начинает кипеть при температуре 100 градусов Цельсия. Чем выше над уровнем моря находится место, тем ниже будет температура кипения воды.
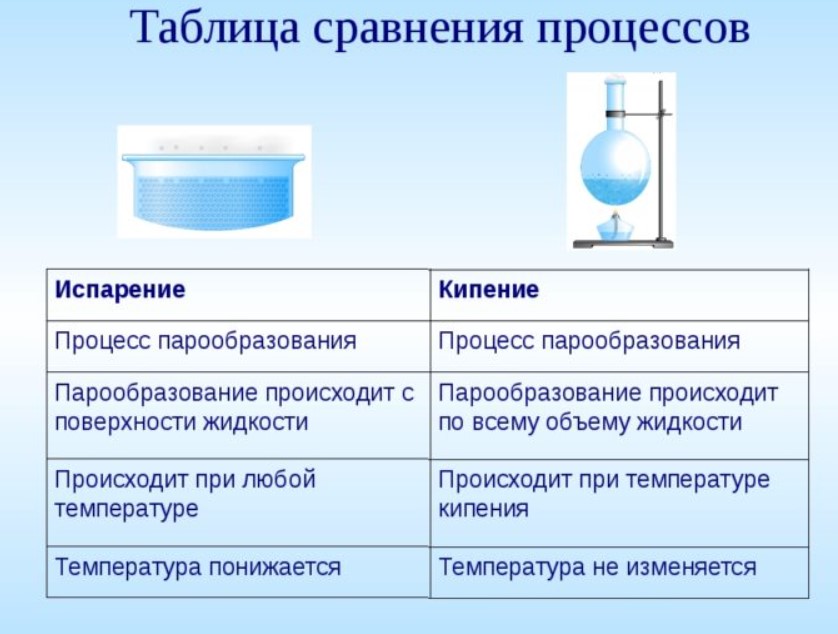
Переход из жидкого состояния в газообразное сопровождается образованием пузырьков пара, которые поднимаются вверх и разрываются на поверхности жидкости. Это явление называется кипением. В процессе кипения происходит поглощение теплоты, что позволяет жидкости испаряться при достижении определенной температуры, несмотря на то, что она может быть ниже точки кипения. Пар, образующийся при кипении, содержит молекулы жидкости или растворенных в ней веществ, которые переходят в газовое состояние.
Атмосферное кипение является одним из фундаментальных процессов в природе и имеет различные применения в жизни человека. Например, благодаря атмосферному кипению вода в котле начинает закипать, что позволяет приготовить пищу. Также атмосферное кипение используется в процессах испарения, конденсации, адсорбции и других химических реакциях.
Определение
Таблица 1:
| Вещество | Точка кипения (°C) |
|---|---|
| Вода | 100 |
| Этанол | 78 |
| Ацетон | 56 |
| Сера | 444 |
| Метанол | 65 |
Точка кипения имеет важное значение во многих процессах и применениях, таких как приготовление пищи, производство лекарств, научные исследования и т.д. Понимание точки кипения помогает контролировать и предсказывать поведение жидкостей при различных условиях.
Температура точки кипения
Точка кипения является характеристикой каждого вещества. Например, для воды точка кипения при нормальном атмосферном давлении составляет 100 градусов Цельсия. Однако, с изменением давления точка кипения может изменяться. При повышении давления точка кипения увеличивается, а при уменьшении — уменьшается.
Точка кипения также зависит от чистоты вещества. Например, при добавлении растворителей или примесей к веществу, точка кипения может снижаться или повышаться.
Знание температуры точки кипения важно для многих процессов, включая пищевую промышленность, химическую промышленность, лабораторные исследования и многие другие. Также, точка кипения может использоваться в качестве метода определения чистоты вещества.
Эффекты повышения давления
Повышение давления на жидкость может оказать значительное влияние на ее физические свойства, включая точку кипения. Когда давление на жидкость возрастает, температура, при которой жидкость закипает, также повышается.
Этот эффект называется эффектом повышения давления и объясняется с помощью физического закона, известного как закон Рауля. Согласно закону Рауля, парциальное давление компонента в жидкой смеси пропорционально его фракции молярной доли и парциальному давлению чистого компонента.
Таким образом, если на жидкость оказывается дополнительное внешнее давление, то парциальное давление компонента в жидкости возрастает, и чтобы уравновесить это давление, необходимо повысить температуру. Из-за этого закипание жидкости происходит при более высокой температуре.
Эффект повышения давления является фундаментальным влиянием в различных промышленных и научных областях. Например, он играет значительную роль в процессах кипения и конденсации, а также в процессах, связанных с очисткой и обработкой воды.
Факторы, влияющие на атмосферное кипение
1. Атмосферное давление: Давление на поверхности жидкости оказывает влияние на ее кипение. Чем ниже атмосферное давление, тем ниже температура, при которой начинается кипение. Например, в горах, где атмосферное давление ниже, вода начинает кипеть при более низкой температуре.
2. Взаимодействие молекул: Силы взаимодействия между молекулами влияют на температуру кипения. Молекулы сильно притягиваются друг к другу, то кипение может происходить при более высокой температуре. Например, вода с высоким содержанием соли имеет более высокую температуру кипения из-за сильного взаимодействия молекул.
3. Свойства вещества: Различные вещества имеют различные температуры кипения. Например, вода при комнатной температуре кипит при 100 градусах Цельсия, а спирт — при более низкой температуре. Это связано с разными свойствами молекул и их взаимодействиями.
Важно отметить, что вышеуказанные факторы являются основными, но не исчерпывающими. Влияние других факторов, таких как наличие примесей в жидкости или ее состав, также может повлиять на температуру кипения в атмосфере.
Свойства вещества
Одним из физических свойств вещества является температура, при которой жидкость закипает. Закипание – это фазовый переход, при котором жидкость переходит в газообразное состояние. Температура закипания является индивидуальной для каждого вещества и зависит от атмосферного давления.
Важно отметить, что температура закипания – это температура при нормальном атмосферном давлении, которое составляет примерно 101,3 кПа или 1 атмосферу. При изменении давления, температура закипания может также изменяться.
Закипание – это процесс, необходимый, например, для приготовления пищи или для работы паровых двигателей. Кроме того, температура закипания может использоваться в различных химических и физических экспериментах.
Изучение температуры закипания и других физических свойств вещества является важным аспектом в различных научных и промышленных областях, таких как химия, физика и инженерия. Понимание этих свойств позволяет улучшить процессы производства и разработать новые материалы с нужными характеристиками.
Атмосферное давление
Значение атмосферного давления можно измерять в разных единицах, например, в миллибарах (мбар), гектопаскалях (гПа) или миллиметрах ртутного столба (мм рт.ст.). Обычно используется миллибар или гектопаскаль.
В среднем атмосферное давление на уровне моря составляет около 1013 миллибар или 1013 гектопаскалей. Однако, это значение может меняться в зависимости от многих факторов, включая географическое положение, высоту над уровнем моря, погодные условия и временные изменения атмосферы.
Измерение атмосферного давления проводится с помощью барометра. Барометры бывают анероидные или ртутные. Анероидные барометры основаны на измерении деформации металлического корпуса, а ртутные барометры используют ртуть в стеклянной трубке. С помощью барометров можно определить текущее атмосферное давление и прогнозировать погоду.
Вопрос-ответ:
Какая температура считается точкой кипения для воды?
Температура кипения воды при нормальных условиях (на уровне моря) составляет 100 градусов Цельсия.
Что происходит с жидкостью при ее закипании?
При закипании жидкости ее молекулы получают достаточно энергии для преодоления межмолекулярных сил и переходят из жидкого состояния в газообразное.
Как меняется давление в закипающей жидкости?
В момент закипания давление в закипающей жидкости становится равным атмосферному давлению.
Может ли температура кипения жидкости изменяться в зависимости от внешних условий?
Да, температура кипения жидкости может изменяться в зависимости от изменений внешних условий. Например, при увеличении атмосферного давления точка кипения жидкости повышается, а при уменьшении — понижается.
Почему некоторые жидкости закипают при комнатной температуре, а другие — при высоких температурах?
Температура кипения жидкости зависит от ее химического состава и межмолекулярных сил вещества. Некоторые жидкости имеют слабые межмолекулярные силы и при комнатной температуре уже имеют достаточную энергию для перехода в газообразное состояние, в то время как другие жидкости имеют сильные межмолекулярные силы и требуют более высоких температур для закипания.